มณีแดง (RED-GEMs): นวัตกรรมย้อนวัยระดับดีเอ็นเอโดยศ.ดร.นพ. อภิวัฒน์ มุทิรางกูร #
บทนำ: ทำไมดีเอ็นเอของเราถึง “แก่” #
ความลับของความอ่อนเยาว์ที่ซ่อนอยู่ในรอยแยกดีเอ็นเอ #
ดีเอ็นเอของคนหนุ่มสาวมี “รอยแยก” มากกว่าคนชรา #
การค้นพบที่น่าทึ่งที่สุดอย่างหนึ่งในวงการวิทยาศาสตร์การแพทย์ช่วงทศวรรษที่ผ่านมา คือการที่ทีมวิจัยไทยนำโดย ศ.ดร.นพ. อภิวัฒน์ มุทิรางกูร จากคณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ได้ค้นพบว่า ดีเอ็นเอของคนหนุ่มสาวมี “รอยแยก” หรือช่องว่าง (DNA gaps) มากกว่าดีเอ็นเอของคนชรา ซึ่งเป็นข้อมูลที่ขัดกับความเชื่อแบบดั้งเดิมที่คิดว่าดีเอ็นเอที่สมบูรณ์แบบต้องเป็นสายยาวต่อเนื่องไม่มีขาด
รอยแยกเหล่านี้มีชื่อทางวิทยาศาสตร์ว่า “Youth-DNA-GAPs” หรือ “รอยแยกดีเอ็นเอเยาว์” ซึ่งเป็นช่องว่างธรรมชาติที่เกิดขึ้นบนสายดีเอ็นเอ โดยมีหน้าที่สำคัญในการลดแรงบิดเกลียว (torsional stress) ที่เกิดขึ้นเมื่อดีเอ็นเอทำงาน กล่าวคือ เมื่อดีเอ็นเอถูกถอดรหัสเพื่อสร้างโปรตีน สายดีเอ็นเอจะต้องแยกเป็นสายเดี่ยว ซึ่งทำให้เกิดแรงบิดเกลียวตามมา รอยแยกเหล่านี้จะช่วยบรรเทาแรงบิดได้ ทำให้ดีเอ็นเอไม่ถูกทำลายจากความตึงเครียดที่สะสม

การศึกษาในหลายระดับ ตั้งแต่เซลล์ยีสต์ หนูทดลอง ไปจนถึงมนุษย์ พบว่า เซลล์ที่กำลังแก่ตัวลงตามเวลามีจำนวน DNA gaps ลดลงอย่างชัดเจน นอกจากนี้ยังพบว่าเซลล์ที่เข้าสู่ภาวะหยุดการแบ่งตัวถาวรหรือเซลล์ชรา (senescent cells) ในมนุษย์ รวมถึงหนูที่แก่ตามธรรมชาติและหนูที่ถูกเร่งให้แก่ด้วยสาร D-galactose ต่างก็แสดงระดับ Youth-DNA-GAPs ที่ต่ำกว่าอย่างมีนัยสำคัญ
| กลุ่มตัวอย่าง | อายุ/สภาวะ | ระดับ Youth-DNA-GAPs | หมายเหตุ |
|---|---|---|---|
| หนูวัยหนุ่ม | 5-7 เดือน | สูง (baseline) | ค่าปกติ |
| หนูวัยกลางคน | 7 เดือน | ลดลง | เริ่มมีความเสียหายของดีเอ็นเอ |
| หนูวัยชรา | 30 เดือน | ต่ำมาก | มีเซลล์แก่สะสม |
| หนูที่ถูกกระตุ้นให้แก่เร็ว | 7 เดือน + D-gal | ต่ำเท่ากับหนูวัยชรา | ยืนยันบทบาทของรอยแยกในการชะลอวัย |
| มนุษย์ (n=80) | >35 ปี | สัมพันธ์เชิงลบกับอายุ | ติดตาม 4 ปี (2015-2019) |
รอยแยกเหล่านี้ช่วยลดแรงบิดเกลียว ป้องกันความเสียหาย #
กลไกการปกป้องดีเอ็นเอโดยรอยแยกนั้นซับซ้อนและชาญฉลาดอย่างน่าอัศจรรย์ รอยแยกเหล่านี้ถูก “ซ่อน” โดยกลไกทางอีพิเจเนติกส์ที่เรียกว่า histone deacetylation ซึ่งเป็นการถอดกลุ่มอะซีทิลออกจากโปรตีนฮิสโตนที่ห่อหุ้มดีเอ็นเอ การซ่อนรอยแยกนี้มีความจำเป็นอย่างยิ่งเพราะหากเซลล์ตรวจพบรอยแยกโดยไม่มีกลไกการปกป้อง เซลล์จะเข้าสู่กระบวนการ “ตอบสนองต่อความเสียหายของดีเอ็นเอ” (DNA damage response: DDR) ซึ่งอาจนำไปสู่การหยุดการแบ่งตัวของเซลล์หรือแม้กระทั่งการตายของเซลล์
ทีมวิจัยใช้เปรียบเทียบรอยแยกดีเอ็นเอเยาว์กับ “ช่องว่างเล็กๆ ในรางรถไฟ” ที่ช่วยให้รางสามารถขยายตัวและหดตัวได้เมื่ออุณหภูมิเปลี่ยนแปลง โดยไม่ทำให้รางบิดเบี้ยวหรือหัก ในทำนองเดียวกัน รอยแยกดีเอ็นเอเยาว์ช่วยให้ดีเอ็นเอสามารถเคลื่อนที่และปรับตัวได้เมื่อมีแรงบิดเกิดขึ้น ทำให้โครงสร้างพันธะเคมีของดีเอ็นเอคงทนขึ้นและไม่ถูกทำลายง่าย

นอกจากนี้ การศึกษายังพบว่า โปรตีน SIRT1 ในมนุษย์ ซึ่งเป็นฮอมอลอกของ Sir2 ในเซลล์ยีสต์ มีบทบาทสำคัญในการรักษาระดับของ Youth-DNA-GAPs เซลล์ที่ขาด SIRT1 หรือโปรตีนกลุ่ม HMGB จะมีจำนวนรอยแยกที่ตรวจพบได้น้อยลง ซึ่งสอดคล้องกับการค้นพบว่า SIRT1 และ histone deacetylation ทำงานร่วมกันในการซ่อนรอยแยกและป้องกันการตอบสนองที่ไม่พึงประสงค์
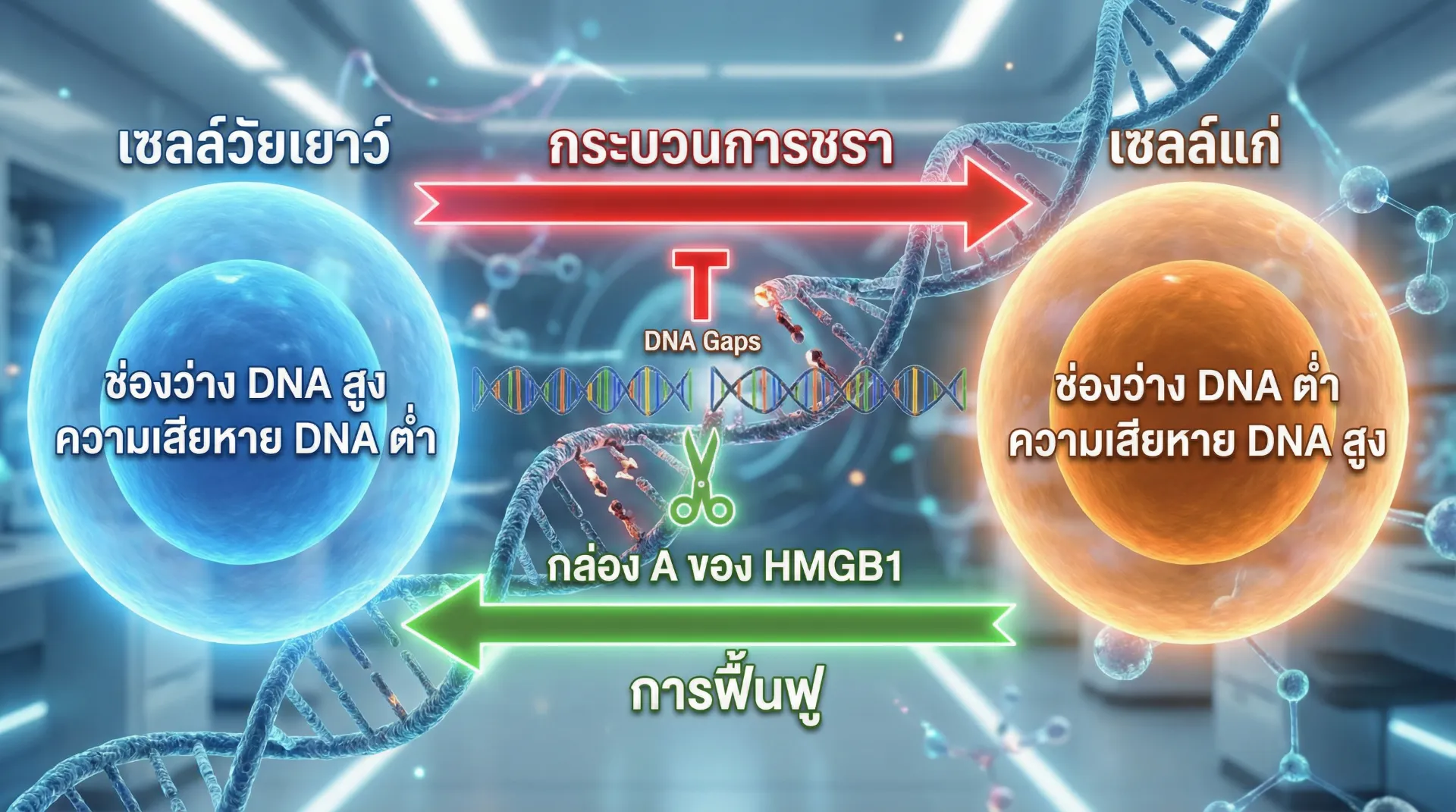
เมื่ออายุมากขึ้น รอยแยกลดลง → ดีเอ็นเอเสียหายง่าย → เซลล์แก่ #
เมื่อรอยแยกดีเอ็นเอเยาว์ลดลงตามอายุ ผลที่ตามมาคือดีเอ็นเอสูญเสียความสามารถในการรับมือกับแรงบิดเกลียว ทำให้เกิดความเสียหายของสายดีเอ็นเอบ่อยขึ้น ความเสียหายเหล่านี้สะสมเป็นจุดที่เรียกว่า “รอยโรคดีเอ็นเอ” (DNA lesions) ซึ่งจะส่งสัญญาณให้เซลล์เข้าสู่ภาวะหยุดการแบ่งตัวถาวรหรือ เซลล์ชรา (cellular senescence)
เซลล์ชราเหล่านี้ยังคงมีชีวิตแต่ไม่สามารถแบ่งตัวได้ และที่สำคัญคือจะ หลั่งสารอักเสบที่เป็นอันตรายต่อเซลล์ข้างเคียง ทำให้เกิดการอักเสบเรื้อรังและการเสื่อมโทรมของเนื้อเยื่อโดยรอบ วัฏจักรนี้กลายเป็นวงจรอุบาทว์ที่ทำให้ร่างกายเสื่อมโทรมตามธรรมชาติ:
รอยแยกลดลง → ดีเอ็นเอเสียหายง่าย → เกิดเซลล์ชราเพิ่มขึ้น
↓
การเสื่อมโทรมของอวัยวะ ← การอักเสบเรื้อรัง ← หลั่งสารอักเสบ (SASPs)
การหยุดวัฏจักรนี้จึงเป็นหัวใจสำคัญของการพัฒนาวิธีการย้อนวัยที่มีประสิทธิภาพ
การค้นพบครั้งสำคัญของทีมวิจัยไทย #
ศ.ดร.นพ. อภิวัฒน์ มุทิรางกูร และทีมวิจัย คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย #
ศาสตราจารย์ ดอกเตอร์ แพทย์ อภิวัฒน์ มุทิรางกูร เป็นผู้เชี่ยวชาญด้านพันธุศาสตร์โมเลกุลและอีพิเจเนติกส์ และเป็นหัวหน้าภาควิชากายวิภาคศาสตร์ คณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ท่านมีผลงานวิจัยที่ได้รับการยอมรับในระดับนานาชาติมากมาย รวมถึงการค้นพบกลไกของ uniparental disomy ของโครโมโซม 15 การตรวจหา DNA ของไวรัส Epstein-Barr ในเลือดสำหรับการวินิจฉัยมะเร็งจมูก การศึกษาบทบาทของ LINE-1 และ Alu methylation ในชีววิทยาและโรคของมนุษย์ รวมถึงการค้นพบบทบาทอีพิเจเนติกส์ของ RIND-EDSBs (physiologic DNA breaks) ในการป้องกันความเสียหายของดีเอ็นเอ
ทีมวิจัยของศ.อภิวัฒน์ประกอบด้วยนักวิจัยรุ่นใหม่ที่มีความสามารถ อาทิ ดร.ศรียะ ยะสม (Sikrit Yasom) ผู้เขียนบทความหลักในวารสาร FASEB BioAdvances ดร.ปาปิชญา วัชรานุรักษ์ (Papitchaya Watcharanurak) และนักวิจัยอื่นๆ จากศูนย์ความเป็นเลิศด้านพันธุศาสตร์โมเลกุลของมะเร็งและโรคในมนุษย์ การค้นพบล่าสุดเกี่ยวกับ Youth-DNA-GAPs และการประยุกต์ใช้ Box A ของ HMGB1 ถือเป็นความก้าวหน้าที่สำคัญที่สุดในอาชีพวิจัยของศ.อภิวัฒน์

ทฤษฎีใหม่ที่ควบคุมการแก่ของดีเอ็นเอ — ไม่มีใครเคยรู้มาก่อน #
สิ่งที่ทำให้การค้นพบนี้มีความพิเศษและไม่เหมือนใครในโลกคือ ทีมวิจัยไทยได้ค้นพบ “ทฤษฎีใหม่ที่ควบคุมการแก่ของดีเอ็นเอ” ซึ่งไม่เคยมีใครรู้มาก่อน ทฤษฎีนี้อธิบายว่าทำไมดีเอ็นเอถึงแก่ตัวลง และที่สำคัญกว่านั้นคือ ชี้ให้เห็นว่า สามารถ “ย้อนวัย” ดีเอ็นเอได้อย่างไร
ความรู้นี้ไม่มีอยู่ในต่างประเทศ ทำให้ประเทศไทยมีความได้เปรียบในการพัฒนานวัตกรรมด้านนี้ก่อนใคร ทฤษฎีใหม่นี้สรุปได้ว่า: การแก่ของดีเอ็นเอไม่ใช่เพียงผลจากการสะสมของความเสียหายตามเวลา แต่เป็นกระบวนการที่ควบคุมได้ซึ่งเกี่ยวข้องกับการลดลงของรอยแยกดีเอ็นเอเยาว์ที่มีหน้าที่ปกป้องดีเอ็นเอ การเข้าใจกลไกนี้ทำให้สามารถออกแบบการแทรกแซงที่ตรงจุดและมีประสิทธิภาพ โดยไม่ใช่เพียงแค่พยายามซ่อมแซมความเสียหายที่เกิดขึ้นแล้ว แต่เป็นการป้องกันไม่ให้ความเสียหายเกิดขึ้นตั้งแต่แรก
ความร่วมมือกับ ปตท. เพื่อพัฒนาเป็นผลิตภัณฑ์รักษาโรค #
ในปี 2022 บริษัท ปตท. จำกัด (มหาชน) ซึ่งเป็นบริษัทพลังงานระดับชาติของไทย ได้ลงนามในบันทึกข้อตกลงความร่วมมือกับจุฬาลงกรณ์มหาวิทยาลัย เพื่อพัฒนาและผลิต “ดีเอ็นเอย้อนวัย” ให้กลายเป็นผลิตภัณฑ์รักษาโรคที่สามารถใช้ได้จริง ความร่วมมือนี้มีเป้าหมายที่ทะเยอทะยานไม่เพียงแค่ช่วยเหลือผู้สูงอายุให้มีสุขภาพดีขึ้น แต่ยังต้องการ สร้าง “รายได้ให้ประเทศไทย” จากการเป็นผู้นำด้านนวัตกรรมต้านความชราระดับโลก
ศ.อภิวัฒน์กล่าวว่าการค้นพบนี้สามารถนำไปใช้รักษาปัญหาสุขภาพที่เกี่ยวข้องกับความชราได้หลายอย่าง และความร่วมมือกับ ปตท. จะช่วยให้ RED-GEMs สามารถเข้าสู่ตลาดได้เร็วขึ้น การที่บริษัทขนาดใหญ่ระดับชาติเข้ามาสนับสนุนการวิจัยนี้แสดงให้เห็นถึงศักยภาพทางการค้าที่สำคัญและความน่าเชื่อถือของผลงานวิจัย
มณีแดงคืออะไร? (RED-GEMs: REjuvenating DNA by GEnomic Stability Molecules) #

ความหมายและที่มาของชื่อ #
RED-GEMs = โมเลกุลฟื้นฟูดีเอ็นเอผ่านความเสถียรของจีโนม #
RED-GEMs ย่อมาจาก “REjuvenating DNA by GEnomic Stability Molecules” ซึ่งแปลตรงตัวว่า “โมเลกุลที่ฟื้นฟูดีเอ็นเอผ่านความเสถียรของจีโนม” ชื่อนี้สะท้อนถึงกลไกการทำงานหลักของนวัตกรรมนี้ นั่นคือ การเสริมสร้างความเสถียรของจีโนม (ชุดดีเอ็นเอทั้งหมดของเซลล์) เพื่อให้ดีเอ็นเอสามารถทำงานได้อย่างมีประสิทธิภาพเหมือนในวัยหนุ่มสาว
ความแตกต่างสำคัญระหว่าง RED-GEMs กับวิธีการรักษาความชราอื่นๆ คือ มันไม่ได้พยายามแก้ไขความเสียหายที่เกิดขึ้นแล้ว แต่เป็นการป้องกันไม่ให้ความเสียหายเกิดขึ้นตั้งแต่แรก โดยการเติมเต็มสิ่งที่ร่างกายสูญเสียไปตามธรรมชาติเมื่ออายุมากขึ้น นั่นคือ “รอยแยกดีเอ็นเอเยาว์” ที่มีหน้าที่ปกป้องดีเอ็นเอจากความเสียหาย
ภาษาไทยเรียก “มณีแดง” — สื่อถึงความสำคัญและคุณค่า #
ในภาษาไทย นวัตกรรมนี้ถูกเรียกว่า “มณีแดง” ซึ่งเป็นชื่อที่สื่อถึงความสำคัญและคุณค่าของการค้นพบนี้ เหมือนกับอัญมณีล้ำค่าสีแดง ชื่อนี้ยังสะท้อนถึง ความภาคภูมิใจที่เป็นนวัตกรรมจากฝีมือคนไทย ไม่ใช่การนำเข้าหรือเลียนแบบจากต่างประเทศ
การตั้งชื่อภาษาไทยที่เข้าใจง่ายนี้ยังช่วยให้ประชาชนทั่วไปสามารถเข้าถึงและเข้าใจนวัตกรรมทางวิทยาศาสตร์ที่ซับซ้อนได้ง่ายขึ้น โดยไม่ต้องใช้ศัพท์เทคนิคที่ยากต่อการจดจำ มณีแดงจึงกลายเป็นสัญลักษณ์ของความหวังในการมีสุขภาพดีและอายุยืนที่คนไทยสามารถเข้าถึงได้

โครงสร้างของมณีแดง #
ส่วนประกอบหลัก: Box A plasmid ห่อหุ้มด้วย Calcium Phosphate nanoparticle #
มณีแดงมีโครงสร้างที่ถูกออกแบบมาอย่างพิถีพิถันเพื่อให้สามารถส่งตัวยาที่มีประสิทธิภาพไปยังเซลล์เป้าหมายได้อย่างปลอดภัยและมีประสิทธิภาพ ส่วนประกอบหลักประกอบด้วยสองส่วน:
| ส่วนประกอบ | รายละเอียด | หน้าที่ |
|---|---|---|
| Box A plasmid | DNA ที่มีลำดับยีนของ Box A จาก HMGB1 | เมื่อเข้าสู่เซลล์ เซลล์จะสังเคราะห์โปรตีน Box A ออกมาทำงาน |
| Calcium Phosphate nanoparticle | นาโนอนุภาคแคลเซียมฟอสเฟตที่ห่อหุ้ม plasmid | ปกป้อง plasmid ช่วยในการส่งเข้าสู่เซลล์ มีความปลอดภัยสูง |
การใช้ plasmid แทนการฉีดโปรตีนสำเร็จรูปมีข้อได้เปรียบหลายประการ: โปรตีนที่สังเคราะห์ภายในเซลล์จะมีการพับตัวที่ถูกต้อง สามารถควบคุมปริมาณได้ตามการแสดงออกของยีน และมีความเสถียรสูงกว่าโปรตีนบริสุทธิ์ นอกจากนี้ยังสามารถผลิตในปริมาณมากได้ง่ายกว่า ซึ่งสำคัญสำหรับการพัฒนาเป็นผลิตภัณฑ์เชิงพาณิชย์
เทคโนโลยีคล้ายวัคซีน mRNA ที่ใช้กันในปัจจุบัน #
การใช้เทคโนโลยี nanoparticle ในการส่งสารพันธุกรรมเข้าไปในเซลล์นั้น ได้รับความสนใจอย่างมากในช่วงการระบาดของโควิด-19 เนื่องจากวัคซีน mRNA ของ Pfizer-BioNTech และ Moderna ใช้เทคโนโลยี lipid nanoparticle ที่คล้ายคลึงกัน ความสำเร็จของวัคซีนเหล่านี้ได้พิสูจน์ว่า เทคโนโลยีการส่งสารพันธุกรรมเข้าไปในเซลล์สามารถทำได้อย่างปลอดภัยในมนุษย์จำนวนมหาศาล
ทีมวิจัยของศ.อภิวัฒน์เลือกใช้ Calcium Phosphate nanoparticle เนื่องจาก:
- มีความปลอดภัยสูง เป็นสารที่พบได้ตามธรรมชาติในร่างกาย (กระดูก ฟัน)
- มีประวัติการใช้งานในการส่งยาเข้าไปในเซลล์มายาวนาน
- สามารถผลิตได้ง่ายและมีต้นทุนต่ำกว่าเทคโนโลยีอื่น
- ไม่ก่อให้เกิดภูมิต้านทานเหมือน lipid nanoparticle บางชนิด
ซึ่งสอดคล้องกับเป้าหมายในการทำให้มณีแดงเข้าถึงได้สำหรับประชาชนทั่วไปในอนาคต
ส่งตรงไปยังเซลล์เป้าหมาย ปลอดภัย มีประสิทธิภาพ #
ระบบการส่งมอบ (delivery system) ของมณีแดงถูกออกแบบให้สามารถเข้าไปในเซลล์ได้หลายประเภท ไม่จำกัดเฉพาะเซลล์บางชนิด ซึ่งมีความสำคัญเนื่องจาก ความชราเป็นกระบวนการที่เกิดขึ้นในทุกอวัยวะและทุกประเภทของเซลล์ ความสามารถในการเข้าถึงเซลล์หลากหลายประเภททำให้มณีแดงมีศักยภาพในการ ย้อนวัยระดับร่างกายทั้งหมด (systemic rejuvenation) ไม่ใช่เพียงแค่บางอวัยวะ
การทดสอบความปลอดภัยในสัตว์ทดลองหลายระดับ ตั้งแต่หนู หมู ไปจนถึงลิง แสดงให้เห็นว่ามณีแดงไม่ก่อให้เกิดผลข้างเคียงที่เป็นอันตราย โดยเฉพาะการทดสอบในหมูที่พบว่า เนื้อมีคุณภาพดีขึ้นและไม่พบสารตกค้างที่เป็นอันตราย ซึ่งเป็นข้อมูลสำคัญในการสนับสนุนการทดลองในมนุษย์ต่อไป
HMGB1 และกล่อง A (Box A): กรรไกรโมเลกุลที่สร้างความอ่อนเยาว์ #
HMGB1 (High Mobility Group Box-1) คืออะไร #
โปรตีนธรรมชาติในร่างกายที่มีบทบาทสำคัญ #
HMGB1 (High Mobility Group Box-1) หรือที่เรียกในภาษาไทยว่า “มณีแดง” เป็นโปรตีนที่พบได้ตามธรรมชาติในร่างกายของสัตว์เลี้ยงลูกด้วยนมเกือบทุกชนิด รวมถึงมนุษย์ ชื่อ “High Mobility Group” มาจากคุณสมบัติทางอิเล็กโตรโฟรีซิสที่ทำให้โปรตีนนี้เคลื่อนที่เร็วในเจล ซึ่งสะท้อนถึงโครงสร้างที่ขนาดเล็กและมีประจุไฟฟ้าที่เป็นเอกลักษณ์
HMGB1 เป็นสมาชิกของครอบครัวโปรตีน HMGB ที่มีอยู่หลายชนิด โดยแต่ละชนิดมีบทบาทที่แตกต่างกันแต่เกี่ยวข้องกับการควบคุมโครงสร้างและการทำงานของดีเอ็นเอ โปรตีนในกลุ่มนี้มีลักษณะเด่นคือ สามารถจับกับดีเอ็นเอที่มีรูปทรงที่ถูกบิดเบี้ยว (distorted DNA structures) ได้อย่างมีความจำเพาะสูง ทำให้มีบทบาทสำคัญในการจัดเรียงโครงสร้างของโครมาติน (chromatin remodeling) และการควบคุมการอ่านข้อมูลจากดีเอ็นเอ
ทำหน้าที่รักษาความเสถียรของดีเอ็นเอ และซ่อมแซมความเสียหาย #
ในสภาวะปกติ HMGB1 ทำหน้าที่หลักในนิวเคลียสของเซลล์ โดยมีบทบาทสำคัญหลายประการ:
1. การรักษาโครงสร้างของโครมาติน HMGB1 ช่วยให้ดีเอ็นเองอตัวและจัดเรียงตัวในรูปแบบที่เหมาะสมสำหรับการทำงาน ซึ่งมีความจำเป็นสำหรับการถอดรหัสยีน การทำซ้ำดีเอ็นเอ และการซ่อมแซมความเสียหาย โปรตีนนี้สามารถ งอดีเอ็นเอ (DNA bending) ได้มากกว่า 90 องศา ช่วยให้ดีเอ็นเอสามารถพับเก็บในนิวเคลียสที่มีขนาดจำกัด และช่วยให้โปรตีนอื่นๆ เข้าถึงลำดับดีเอ็นเอเป้าหมายได้ง่ายขึ้น
2. การซ่อมแซมความเสียหายของดีเอ็นเอ HMGB1 สามารถจับกับจุดที่ดีเอ็นเอถูกบิดงอหรือเสียหาย ช่วยให้เอนไซม์ซ่อมแซมสามารถเข้าถึงและแก้ไขความเสียหายได้ง่ายขึ้น นอกจากนี้ยังมี กิจกรรม deoxyribose phosphate lyase ซึ่งเป็นขั้นตอนสำคัญในการซ่อมแซมดีเอ็นเอแบบ base excision repair
การควบคุมการทำงานของยีน โดยการเปลี่ยนแปลงโครงสร้างของโครมาติน HMGB1 สามารถช่วยเปิดหรือปิดการทำงานของยีนบางชนิดได้ ทำหน้าที่เป็น ตัวเพิ่มประสิทธิภาพการถอดรหัส (transcription enhancer) และ ปัจจัยการถอดรหัด (transcription factor)
นอกจากบทบาทในนิวเคลียสแล้ว HMGB1 ยังสามารถถูกขับออกนอกเซลล์ได้ในสภาวะที่เซลล์ได้รับความเสียหายหรือตาย โดยมีบทบาทเป็นตัวกลางการอักเสบ (inflammatory mediator) ซึ่งเป็นส่วนหนึ่งของระบบภูมิคุ้มกันของร่างกาย อย่างไรก็ตาม บทบาทนี้แตกต่างจากบทบาทหลักในการรักษาความเสถียรของดีเอ็นเอ และเป็นสิ่งที่ทีมวิจัยต้องคำนึงถึงในการออกแบบมณีแดง
ประกอบด้วยโดเมนสำคัญ 2 ส่วน: Box A และ Box B #
โครงสร้างของ HMGB1 ประกอบด้วยโดเมนหลักสองส่วนที่มีลักษณะเป็นกล่อง (box) ซึ่งเป็นที่มาของชื่อ “Box A” และ “Box B” นอกจากนี้ยังมีส่วนท้ายที่เป็นกรด (acidic C-terminal tail) ที่มีบทบาทในการควบคุมการทำงาน:
| ส่วนประกอบ | ตำแหน่ง (กรดอะมิโอ) | หน้าที่หลัก | ความสำคัญต่อมณีแดง |
|---|---|---|---|
| Box A | ~1-79 | สร้างรอยแยกดีเอ็นเอเยาว์ ปกป้องดีเอ็นเอจากความเสียหาย | ใช้เป็นส่วนประกอบหลัก มีฤทธิ์ย้อนวัย ไม่ก่อการอักเสบ |
| Box B | ~89-163 | จับดีเอ็นเอที่บิดเบี้ยว เกี่ยวข้องกับการอักเสบเมื่อหลั่งออกนอกเซลล์ | ไม่ใช้ เนื่องจากก่อให้เกิดการอักเสบ |
| Acidic C-tail | ~186-215 | ควบคุมการงอตัวของดีเอ็นเอ ปรับแต่งการทำงานของ Box A และ Box B | มีบทบาทในการควบคุมโครงสร้างโมเลกุล |
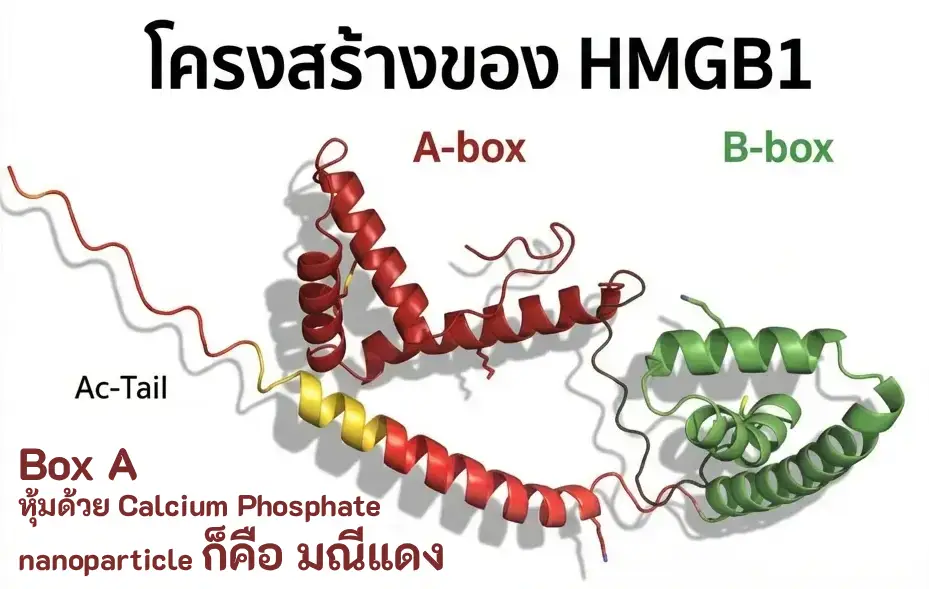
ความแตกต่างระหว่าง Box A และ Box B มีความสำคัญอย่างยิ่งต่อการออกแบบมณีแดง เนื่องจากทีมวิจัยพบว่า Box A มีบทบาทเฉพาะเจาะจงในการสร้างรอยแยกดีเอ็นเอเยาว์ ในขณะที่ Box B มีแนวโน้มที่จะก่อให้เกิดการอักเสบเมื่ออยู่นอกเซลล์ การเลือกใช้เฉพาะ Box A จึงเป็นกุญแจสำคัญในการสร้างผลิตภัณฑ์ที่มีประสิทธิภาพและปลอดภัย
โครงสร้างของ HMGB1 #
Box A (กล่อง A): โดเมนที่มีหน้าที่สร้างรอยแยกดีเอ็นเอ #
Box A ของ HMGB1 เป็นโดเมน N-terminal ที่มีโครงสร้างเป็น HMG-box motif ประกอบด้วยประมาณ 79 กรดอะมิโน จัดเรียงในรูปแบบที่เรียกว่า “HMG-box fold” ซึ่งประกอบด้วย สามฮีลิกซ์อัลฟา (α-helices) ที่พับตัวเป็นรูปตัว L หรือ V สร้างพื้นผิวที่สามารถจับกับดีเอ็นเอในร่องเล็ก (minor groove) ได้อย่างแน่นหนา
คุณสมบัติที่สำคัญที่สุดของ Box A ที่ทีมวิจัยค้นพบคือ ความสามารถในการ “ตัด” สายดีเอ็นเอ สร้างรอยแยกที่มีลักษณะเฉพาะ ซึ่งถูกเรียกว่า “Youth-DNA-GAPs” การตัดนี้ไม่ใช่การตัดแบบสุ่ม แต่เป็นการตัดในตำแหน่งที่มีลักษณะเฉพาะทางลำดับ (sequence-specific) และสภาวะโครงสร้าง (structure-specific) ที่ช่วยให้รอยแยกที่เกิดขึ้นสามารถทำหน้าที่ปกป้องดีเอ็นเอได้อย่างมีประสิทธิภาพ
จุดสำคัญใน Box A คือ กรดอะมิโน Phe38 (ฟีนิลอลานิน ตำแหน่ง 38) ในมนุษย์ หรือ Phe37 ในหนู ซึ่งมีบทบาทสำคัญในการ งอและตัดดีเอ็นเอ การศึกษาโดยใช้การกลายพันธุ์จุด (site-directed mutagenesis) พบว่า:
- Phe38Tyr (F38Y): เปลี่ยนเป็นไทโรซีน มีกิจกรรมสร้างรอยแยกลดลง
- Phe38Trp (F38W): เปลี่ยนเป็นทริปโตเฟาน มีกิจกรรมสร้างรอยแยกลดลงมาก
- Phe38Gly (F38G): เปลี่ยนเป็นไกลซีน ไม่มีกิจกรรมสร้างรอยแยกเลย
นี่แสดงให้เห็นว่า หมู่ฟังก์ชัน aromatic ที่ตำแหน่ง 38 เป็นสิ่งจำเป็นสำหรับกิจกรรมกรรไกรโมเลกุล ของ Box A
Box B (กล่อง B): โดเมนที่เกี่ยวข้องกับการอักเสบ #
Box B เป็นโดเมนกลางของ HMGB1 มีโครงสร้างคล้าย Box A แต่มีหน้าที่ที่แตกต่างกันอย่างสิ้นเชิง โดยเฉพาะเมื่อ HMGB1 หลั่งออกจากเซลล์:
| คุณสมบัติ | Box A | Box B |
|---|---|---|
| กิจกรรมสร้างรอยแยกดีเอ็นเอเยาว์ | มี | ไม่มี |
| ฤทธิ์กระตุ้นการอักเสบ | ไม่มี (antagonist) | มี (agonist) |
| การจับกับ TLR4/RAGE | อ่อน | แรง |
| การใช้ในมณีแดง | ใช้ | ไม่ใช |
Box B มี ความสามารถในการกระตุ้นการอักเสบ (pro-inflammatory activity) สูงกว่า Box A สามารถจับกับตัวรับ TLR4 (Toll-like receptor 4) และ RAGE (Receptor for Advanced Glycation End-products) บนเซลล์ภูมิคุ้มกัน กระตุ้นการหลั่งไซโตไคน์อักเสบ เช่น TNF-α, IL-1, IL-6 ลำดับกรดอะมิโนที่น้อยที่สุดสำหรับฤทธิ์กระตุ้นการอักเสบของ Box B อยู่ที่ตำแหน่ง 89-109
การศึกษาของทีมวิจัยพบว่า Box B ไม่มีกิจกรรมสร้างรอยแยกดีเอ็นเอเยาว์ เมื่อทดสอบในเซลล์ HK-2 และ HEK293 การแสดง Box B อย่างเดียวไม่เพิ่มจำนวนรอยแยกดีเอ็นเอ ในขณะที่ Box A เพิ่มอย่างมีนัยสำคัญ นี่เป็นหลักฐานสำคัญที่สนับสนุนการเลือกใช้ Box A แยก สำหรับการรักษา
หางกรด (Acidic C-tail): ควบคุมการงอตัวของดีเอ็นเอ #
Acidic C-tail หรือ Box C เป็นส่วนท้ายของ HMGB1 ประกอบด้วยกรดอะมิโนกลูตามิกและแอสปาร์ติก 30 ตัวติดต่อกัน ส่วนนี้มีประจุลบสูงและมีบทบาทสำคัญในการควบคุมโครงสร้างสามมิติของ HMGB1
หางกรดช่วย ลดความสามารถในการจับดีเอ็นเอของโดเมน HMG box แต่เป็นสิ่งจำเป็นสำหรับการจับกับดีเอ็นเอที่งอตัว (bent DNA) และการควบคุมกระบวนการเซลล์ต่างๆ เช่น การถ่ายทอดยีนและการหมุนของโครโมโซม (chromosomal derotation) นอกจากนี้ยังมีบทบาทในการจับกับโครมาตินผ่านการมีปฏิสัมพันธ์กับฮิสโตนหลักและฮิสโตนเชื่อม (core and linker histones)
การศึกษาพบว่า การตัดหางกรดออกทำให้ HMGB1 มีความสามารถในการงอดีเอ็นเอมากเกินไป ซึ่งอาจก่อให้เกิดความไม่เสถียรของจีโนมได้ ดังนั้น หางกรดจึงทำหน้าที่เป็น “เบรก” ที่ควบคุมกิจกรรมของ Box A และ Box B
Box A: กรรไกรโมเลกุล (Molecular Scissors) #
ทำหน้าที่ตัดสายดีเอ็นเอ สร้าง “รอยแยกความอ่อนเยาว์” (Youth-DNA-GAPs) #
การค้นพบสำคัญที่สุดของทีมวิจัยศ.ดร.นพ. อภิวัฒน์ คือ Box A ของ HMGB1 ทำหน้าที่เป็น “กรรไกรโมเลกุล” (molecular scissors) ที่สามารถตัดสายดีเอ็นเอเพื่อสร้างรอยแยกดีเอ็นเอเยาว์ได้ กลไกนี้ถูกพิสูจน์ผ่านการทดลองหลายระดับ
ระดับโมเลกุล (in vitro): นำโปรตีน Box A บริสุทธิ์มาสัมผัสกับดีเอ็นเอสายยาว (high-molecular-weight DNA) พบว่า Box A สามารถ สร้างรอยแยกแบบ double-strand breaks (DSBs) ได้ กิจกรรมนี้ขึ้นอยู่กับ Phe38 และไม่พบใน Box B หรือ Box A ที่กลายพันธุ์
ระดับเซลล์ (in cellulo): ถ่ายทอดพลาสมิดที่แสดง Box A เข้าสู่เซลล์ HK-2 และ HEK293 วัดจำนวนรอยแยกดีเอ็นเอโดยเทคนิค ligation-mediated PCR (LM-PCR) พบว่าเซลล์ที่แสดง Box A มีจำนวนรอยแยกเพิ่มขึ้น 2-3 เท่า เทียบกับเซลล์ควบคุม
ระดับสัตว์ (in vivo): ฉีดพลาสมิด Box A เข้าสู่หนูแก่ (30 เดือน) พบว่ารอยแยกดีเอ็นเอเยาว์ในเนื้อเยื่อตับและไตเพิ่มขึ้น สัมพันธ์กับการปรับปรุงตัวชี้วัดความแก่ทุกด้าน

รอยแยกเหล่านี้ซ่อนโดยฮิสโตนที่ถูกดีอะซีทิเลต ป้องกันการตอบสนองของเซลล์ #
รอยแยกดีเอ็นเอที่สร้างโดย Box A ไม่ใช่ความเสียหาย แต่เป็น โครงสร้างที่ได้รับการปกป้อง โดยกลไกทางอีพิเจเนติกส์ การศึกษาพบว่ารอยแยกเหล่านี้ถูก ซ่อนโดยฮิสโตนที่ถูกดีอะซีทิเลต (deacetylated histones) ทำให้โครมาทินหดตัว (heterochromatin formation) และซ่อนรอยแยกจากการตอบสนองของเซลล์ต่อความเสียหายของดีเอ็นเอ (DDR)
กระบวนการซ่อนนี้มีความสำคัญอย่างยิ่ง เพราะหากเซลล์ตรวจพบรอยแยกโดยไม่มีกลไกการปกป้อง เซลล์จะเข้าสู่กระบวนการ ตอบสนองต่อความเสียหายของดีเอ็นเอ (DNA Damage Response: DDR) ซึ่งอาจนำไปสู่การหยุดการแบ่งตัวของเซลล์หรือแม้กระทั่งการตายของเซลล์ การที่รอยแยกถูกซ่อนไว้จึงช่วยให้เซลล์สามารถรักษาความยืดหยุ่นของดีเอ็นเอได้โดยไม่กระตุ้นการตอบสนองที่ไม่พึงประสงค์
ผลลัพธ์: ดีเอ็นเอแข็งแรง ลดความเสียหาย ย้อนวัยเซลล์ #
เมื่อรอยแยกดีเอ็นเอเยาว์ถูกสร้างขึ้นใหม่โดย Box A ผลลัพธ์ที่ตามมาคือ:
| ผลลัพธ์ | กลไก | ผลที่เห็นได้ |
|---|---|---|
| ดีเอ็นเอแข็งแรงขึ้น | ลดแรงบิดเกลียว ป้องกันพันธะเคมีอ่อนแอ | ทนต่อรังสีและสารเคมีดีขึ้น |
| ลดความเสียหายของดีเอ็นเอ | ไม่ต้องเปิดใช้ DDR บ่อยครั้ง | ลด γH2AX, ลดเซลล์แก่ |
| ย้อนวัยเซลล์ | ฟื้นฟูสภาพดีเอ็นเอเหมือนวัยหนุ่ม | เซลล์กลับมาแบ่งตัวได้ ลด SASPs |
กลไกการทำงาน: จากรอยแยกสู่การย้อนวัย #
วัฏจักรความชราที่ธรรมชาติสร้างไว้ #
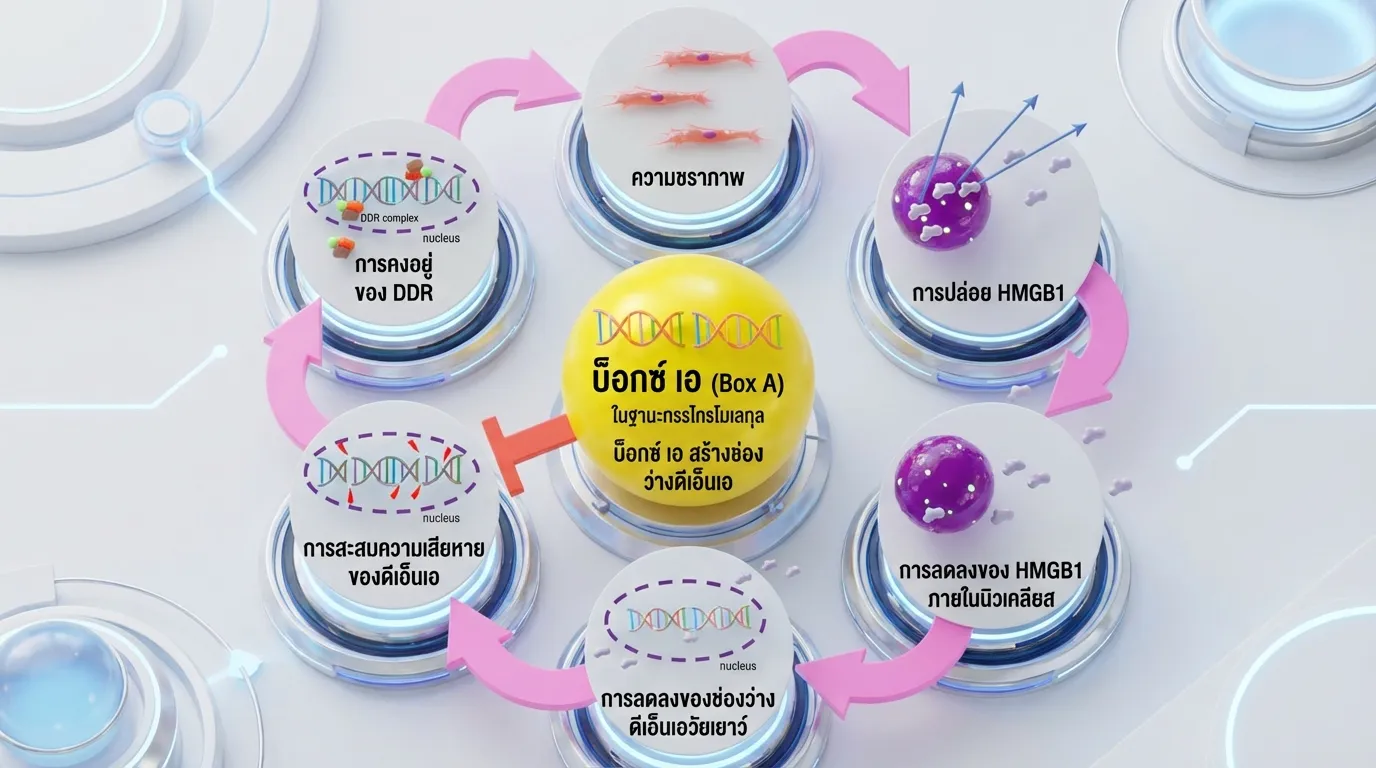
เซลล์แก่ขับ HMGB1 ออกนอกเซลล์ → ขาดโปรตีนสร้างรอยแยก #
กลไกที่ทำให้รอยแยกดีเอ็นเอเยาว์ลดลงเมื่ออายุมากขึ้นเกิดจากการที่ เซลล์ขับโปรตีน HMGB1 ออกไปนอกนิวเคลียส เมื่อเซลล์เริ่มแก่หรือได้รับความเครียด จะมีการขับ HMGB1 ออกจากนิวเคลียสไปสู่ไซโตพลาสซึมและออกสู่ภายนอกเซลล์ ทำให้ภายในนิวเคลียสขาดโปรตีนที่จำเป็นสำหรับการสร้างรอยแยกใหม่
การขับ HMGB1 ออกนอกเซลล์นี้เป็นส่วนหนึ่งของกระบวนการ “immunogenic cell death” หรือการตายของเซลล์ที่กระตุ้นระบบภูมิคุ้มกัน HMGB1 ที่หลั่งออกมาจะทำหน้าที่เป็น DAMP (Damage-Associated Molecular Pattern) กระตุ้นการอักเสบผ่านการจับกับ TLR4 และ RAGE อย่างไรก็ตาม ในระยะยาว การสูญเสีย HMGB1 จากนิวเคลียสทำให้เซลล์ไม่สามารถรักษาระดับรอยแยกดีเอ็นเอเยาว์ได้
ดีเอ็นเอขาดรอยแยก → เกิดความเสียหายสะสม → ส่งสัญญาณให้เซลล์แก่ #
การขาดแคลน HMGB1 ในนิวเคลียสทำให้ไม่สามารถสร้างรอยแยกดีเอ็นเอเยาว์ได้เพียงพอ ผลที่ตามมาคือ แรงบิดเกลียวจากการทำงานของดีเอ็นเอสะสม และทำให้เกิดความเสียหายของดีเอ็นเอมากขึ้น ความเสียหายที่สะสมนี้จะกระตุ้นเส้นทางสัญญาณ DNA Damage Response (DDR) อย่างต่อเนื่อง ซึ่งเป็นสัญญาณให้เซลล์เข้าสู่ภาวะหยุดการแบ่งตัว (cellular senescence) หรือที่เรียกว่า “เซลล์แก่”
เซลล์แก่ที่สะสมอยู่ในเนื้อเยื่อจะหลั่งสารที่เรียกว่า Senescence-Associated Secretory Phenotypes (SASPs) ซึ่งรวมถึงสารก่อการอักเสบต่างๆ เช่น IL-6, IL-8, TNF-α สารเหล่านี้จะส่งสัญญาณให้ระบบภูมิคุ้มกันมากำจัดเซลล์แก่ แต่ในเวลาเดียวกันก็สร้าง ภาวะอักเสบเรื้อรังในเนื้อเยื่อ การสะสมของเซลล์แก่และภาวะอักเสบเรื้อรังนี้เป็นสาเหตุสำคัญที่ทำให้โครงสร้างและหน้าที่ของอวัยวะเสื่อมลงตามอายุ
วัฏจักรนี้ทำให้ร่างกายเสื่อมโทรมตามธรรมชาติ #
วัฏจักรความชราที่ธรรมชาติสร้างไว้สามารถสรุปได้ดังนี้:
อายุมากขึ้น / ความเครียด
↓
HMGB1 ถูกขับออกจากนิวเคลียส
↓
ขาดโปรตีนสร้างรอยแยกดีเอ็นเอเยาว์
↓
รอยแยกลดลง → แรงบิดเกลียวสะสม → ความเสียหายของดีเอ็นเอ
↓
กระตุ้น DDR อย่างต่อเนื่อง → เซลล์เข้าสู่ภาวะ senescence
↓
หลั่ง SASPs → อักเสบเรื้อรัง → การเสื่อมโทรมของอวัยวะ
↓
ความชราที่เห็นได้ชัดในระดับร่างกาย
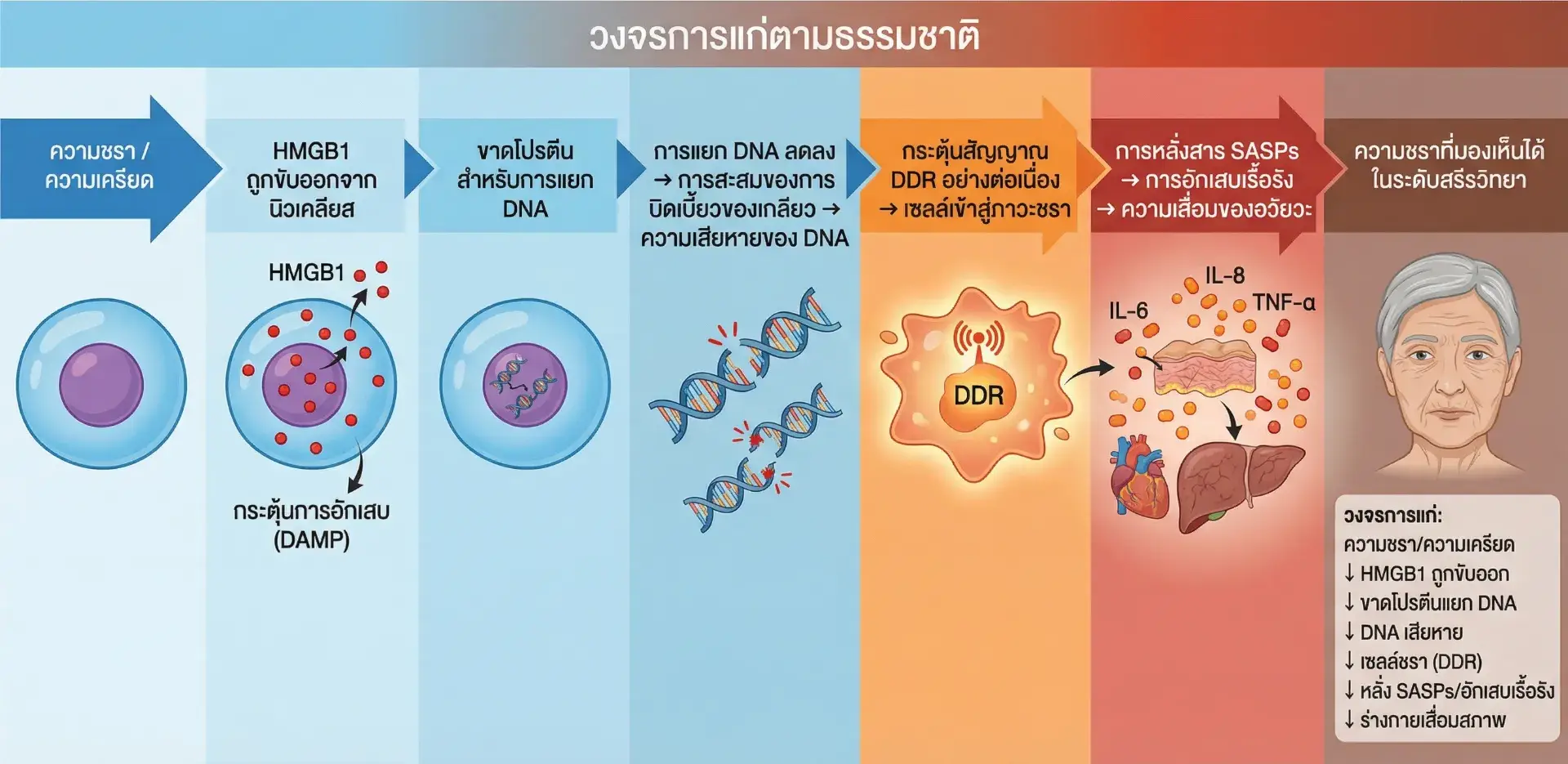
วัฏจักรนี้เกิดขึ้นอย่างหลีกเลี่ยงไม่ได้ตามธรรมชาติ แต่การค้นพบของทีมวิจัยไทยได้เปิดทางให้สามารถ หยุดและย้อนกลับวัฏจักรนี้ได้
มณีแดงหยุดวัฏจักรความชราอย่างไร #
เติม Box A เข้าไปในเซลล์ → สร้างรอยแยกใหม่ #
มณีแดงทำงานโดยการ เติมเต็ม Box A ที่ขาดหายไป เมื่อ plasmid Box A ที่ห่อหุ้มด้วย Calcium Phosphate nanoparticle เข้าสู่เซลล์ เซลล์จะสังเคราะห์โปรตีน Box A ออกมา โปรตีนนี้จะเคลื่อนที่เข้าไปในนิวเคลียสและทำหน้าที่เป็น กรรไกรโมเลกุล สร้างรอยแยกดีเอ็นเอเยาว์ใหม่
ความฉลาดของการออกแบบนี้คือ Box A มีโอกาสน้อยมากที่จะไปทำงานในตำแหน่งที่ไม่ต้องการ (off-target) เนื่องจากการสร้างรอยแยกดีเอ็นเอเยาว์ต้องอาศัยโปรตีนหลายชนิดทำงานร่วมกัน รวมถึง SIRT1 และ AGO4 ดังนั้นแม้ว่าจะมี Box A เกินความจำเป็น ก็ไม่สามารถสร้างรอยแยกในตำแหน่งสุ่มได้
รอยแยกใหม่ช่วยลดแรงบิด ป้องกันความเสียหาย #
เมื่อรอยแยกดีเอ็นเอเยาว์ถูกสร้างขึ้นใหม่ ดีเอ็นเอจะกลับมามีความยืดหยุ่นในการรับมือกับแรงบิดเกลียว ผลที่ตามมาคือ:
- พันธะเคมีของนิวคลีโอไทด์ไม่อ่อนแอลง จากแรงบิดที่สะสม
- ไม่ต้องเปิดใช้ DDR บ่อยครั้ง ซึ่งเป็นสัญญาณของความชรา
- เซลล์สามารถทำงานได้ตามปกติ โดยไม่เข้าสู่ภาวะ senescence
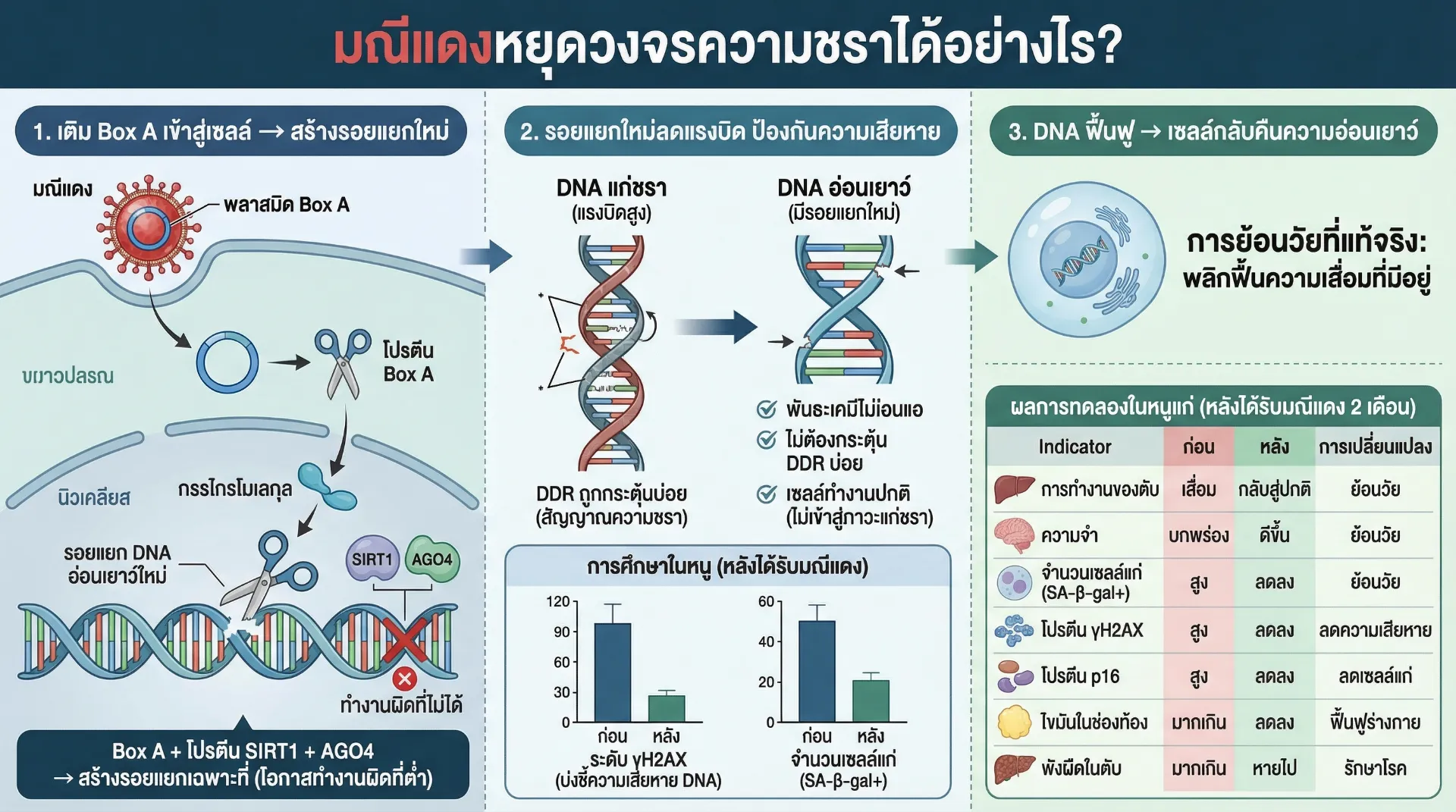
การศึกษาในหนูทดลองพบว่าหลังจากได้รับมณีแดง ระดับ γH2AX (ตัวบ่งชี้ความเสียหายของดีเอ็นเอ) ลดลง และ จำนวนเซลล์แก่ที่ตรวจพบด้วยสี SA-β-gal ลดลงอย่างมีนัยสำคัญ
ดีเอ็นเอกลับมาแข็งแรง → เซลล์ฟื้นคืนสู่สภาพอ่อนเยาว์ #
เมื่อดีเอ็นเอกลับมาแข็งแรงและมีความเสถียร เซลล์จะสามารถ ฟื้นคืนสู่สภาพอ่อนเยาว์ได้จริง ไม่ใช่เพียงแค่หยุดการแก่ชรา แต่เป็นการ ย้อนกลับสภาพที่เสื่อมไปแล้ว ผลการทดลองในหนูแก่พบว่าหลังจากได้รับมณีแดงเป็นเวลา 2 เดือน:
| ตัวชี้วัด | ก่อนรับมณีแดง | หลังรับมณีแดง | การเปลี่ยนแปลง |
|---|---|---|---|
| การทำงานของตับ | เสื่อม | กลับมาปกติ | ย้อนวัย |
| ความจำ | บกพร่อง | ดีขึ้น | ย้อนวัย |
| จำนวนเซลล์แก่ (SA-β-gal+) | สูง | ต่ำลง | ย้อนวัย |
| โปรตีน γH2AX | สูง | ต่ำลง | ลดความเสียหาย |
| โปรตีน p16 | สูง | ต่ำลง | ลดเซลล์แก่ |
| ไขมันในช่องท้อง | สะสมมาก | ลดลง | ฟื้นฟูสภาพร่างกาย |
| พังผืดในตับ | มีมาก | หายไป | รักษาโรค |
ความแตกต่างจากวิธีอื่น #
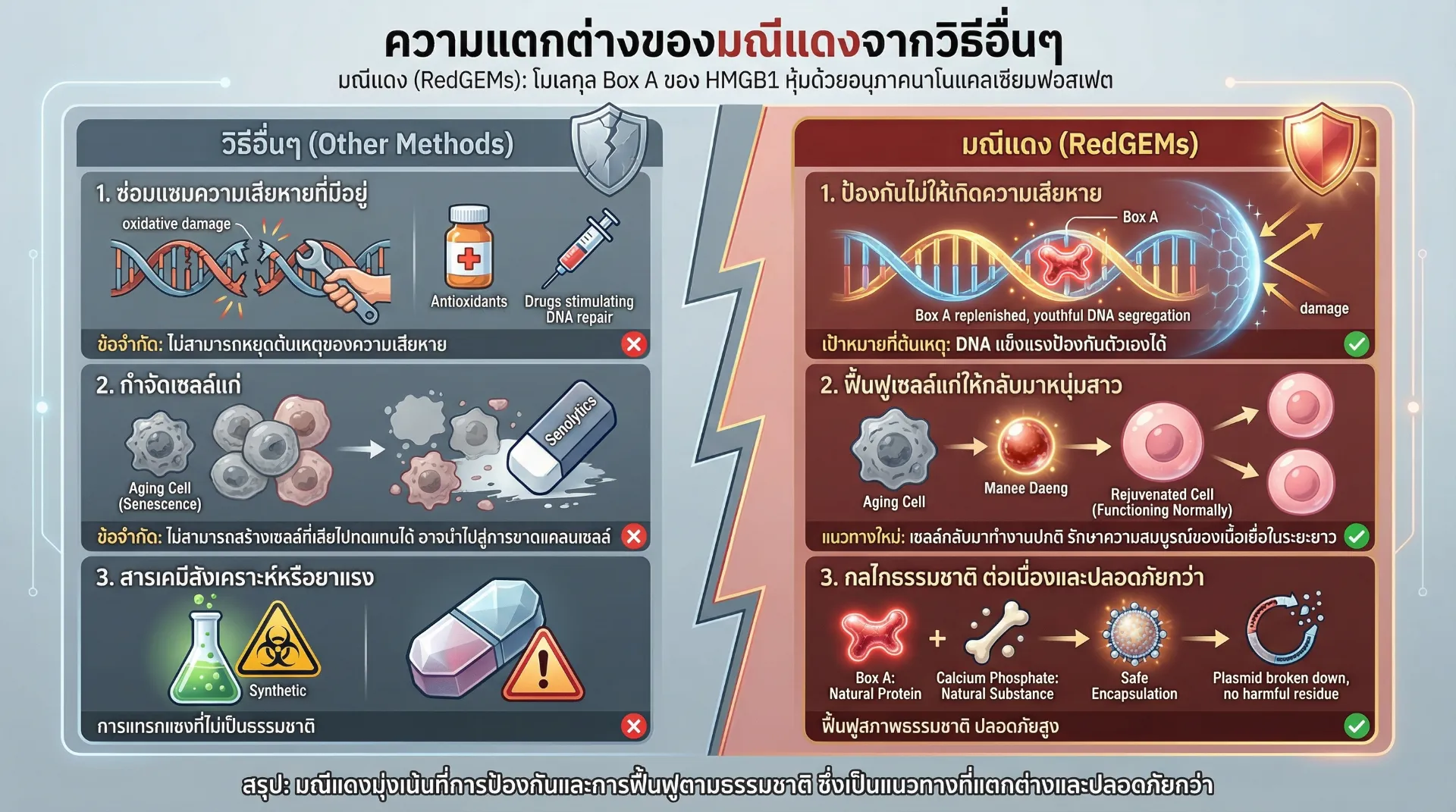
ไม่ใช่การซ่อมแซมความเสียหายที่เกิดแล้ว แต่เป็นการป้องกันไม่ให้เกิด #
วิธีการรักษาความชราที่มีอยู่ในปัจจุบันส่วนใหญ่มุ่งเน้นไปที่ การซ่อมแซมความเสียหายที่เกิดขึ้นแล้ว เช่น การใช้สารต้านอนุภาคอิสระ (antioxidants) เพื่อลดความเสียหายจากออกซิเดชัน หรือการใช้ยาที่กระตุ้นกระบวนการซ่อมแซมดีเอ็นเอ อย่างไรก็ตาม วิธีเหล่านี้มีข้อจำกัดคือ ไม่สามารถหยุดสาเหตุที่ทำให้เกิดความเสียหายได้
มณีแดงแตกต่างอย่างสิ้นเชิง เพราะ มุ่งเป้าไปที่สาเหตุพื้นฐาน คือการขาดรอยแยกดีเอ็นเอเยาว์ที่ทำให้ดีเอ็นเอเสียหายง่าย โดยการเติมเต็ม Box A เข้าไป ดีเอ็นเอจะกลับมามีความแข็งแรงและสามารถ ป้องกันตนเองจากความเสียหายได้ ไม่ใช่เพียงแค่รอให้ความเสียหายเกิดแล้วค่อยซ่อมแซม
ไม่ใช่การกำจัดเซลล์แก่ แต่เป็นการทำให้เซลล์แก่กลับมาหนุ่ม #
อีกวิธีหนึ่งที่กำลังได้รับความสนใจคือ การใช้ senolytics เพื่อกำจัดเซลล์แก่ วิธีนี้สามารถลดภาวะอักเสบเรื้อรังและชะลอการเสื่อมของอวัยวะได้ แต่มีข้อจำกัดคือ ไม่สามารถฟื้นฟูเซลล์ที่สูญเสียไปแล้ว และในระยะยาวอาจทำให้เนื้อเยื่อขาดเซลล์
มณีแดงใช้แนวทางที่แตกต่าง: แทนที่จะกำจัดเซลล์แก่ มันทำให้เซลล์แก่กลับมาอ่อนเยาว์ได้ เซลล์ที่เข้าสู่ภาวะ senescence สามารถกลับมาแบ่งตัวและทำงานได้ตามปกติ ซึ่งเป็นการรักษาความสมบูรณ์ของเนื้อเยื่อในระยะยาว
กลไกต่อเนื่องจากธรรมชาติ ปลอดภัยกว่าวิธีอื่น #
มณีแดงใช้ Box A ซึ่งเป็นโปรตีนธรรมชาติในร่างกาย ไม่ใช่สารเคมีสังเคราะห์หรือยาที่มีฤทธิ์รุนแรง กลไกการทำงานของ Box A เป็นกระบวนการที่เกิดขึ้นตามธรรมชาติในเซลล์อ่อนเยาว์ ดังนั้น การเติมเต็ม Box A จึงเป็นการฟื้นฟูสภาวะธรรมชาติ ไม่ใช่การแทรกแซงด้วยวิธีที่ผิดธรรมชาติ
นอกจากนี้ การใช้ plasmid ที่ห่อหุ้มด้วย Calcium Phosphate nanoparticle ยังมีความปลอดภัยสูง เพราะ แคลเซียมฟอสเฟตเป็นสารที่มีอยู่ตามธรรมชาติในร่างกาย และ plasmid จะถูกย่อยสลายหลังจากเซลล์สังเคราะห์โปรตีน Box A เสร็จสิ้น ไม่มีสารตกค้างที่เป็นอันตราย
ผลการวิจัยของศ.ดร.นพ. อภิวัฒน์ มุทิรางกูร #
การทดลองในหนูทดลอง #
หนูแก่ (30 เดือน) ได้รับมณีแดง 1 ครั้ง/สัปดาห์ นาน 2 เดือน #
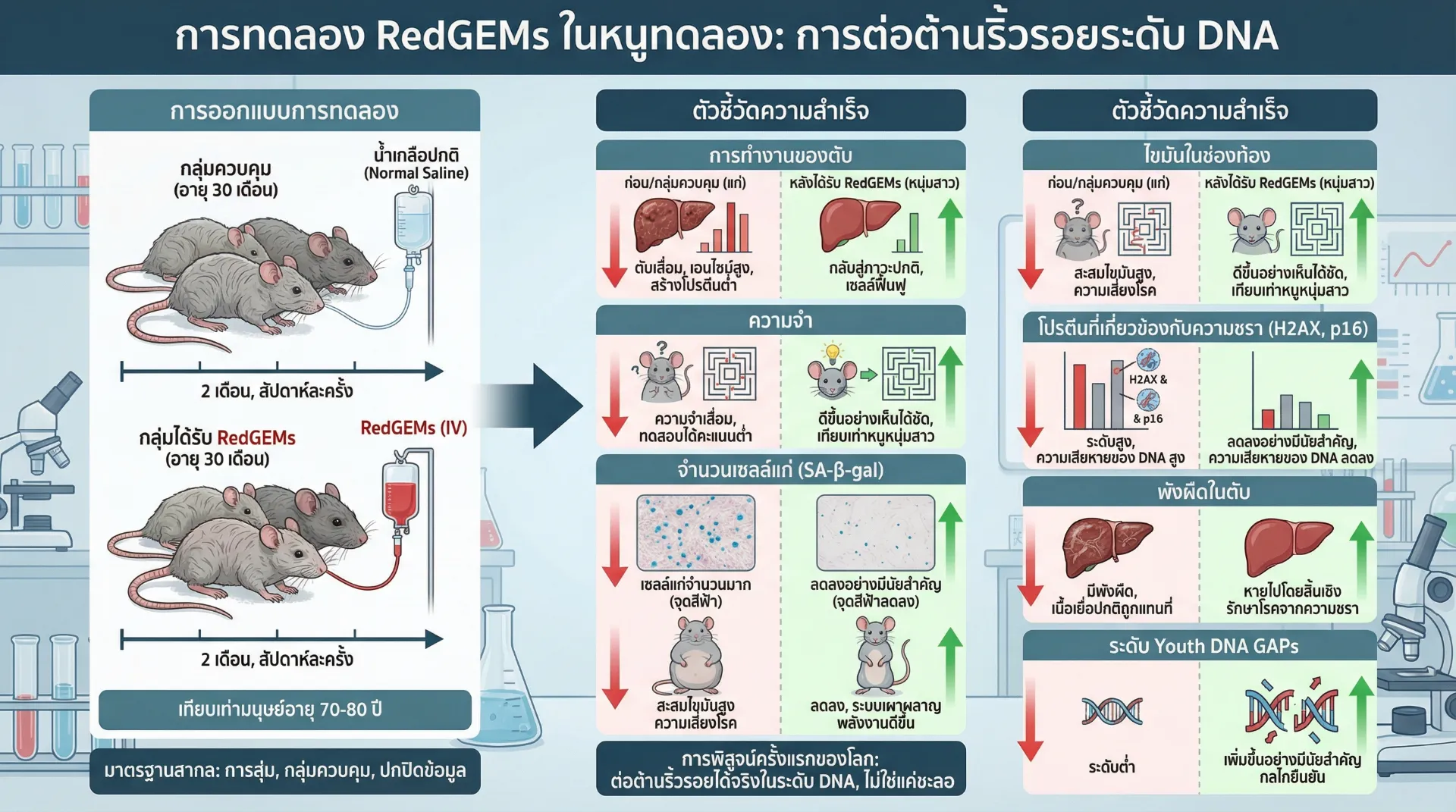
การทดลองสำคัญที่สุดของทีมวิจัยคือการให้ มณีแดงกับหนูแก่อายุ 30 เดือน (เทียบเท่ามนุษย์อายุประมาณ 70-80 ปี) โดยฉีดเข้าทางหลอดเลือดดำ 1 ครั้งต่อสัปดาห์ เป็นเวลา 2 เดือน หนูในกลุ่มควบคุมได้รับสารละลายเกลือ (normal saline)
การออกแบบการทดลองนี้มีความเข้มงวดตามมาตรฐานวิจัยระดับสากล โดยมีการสุ่มกลุ่ม (randomization) มีกลุ่มควบคุม (control group) และมีการตรวจสอบแบบซ่อนชื่อ (blinding) เพื่อให้ได้ผลลัพธ์ที่น่าเชื่อถือที่สุด
ผลลัพธ์: ย้อนวัยได้สมบูรณ์ในทุกด้านที่ทดสอบ #
ผลการทดลองที่ได้น่าทึ่งอย่างยิ่ง: หนูที่ได้รับมณีแดงแสดงการย้อนวัยในทุกด้านที่ทดสอบ โดยไม่พบผลข้างเคียงที่เป็นอันตราย นี่เป็นการพิสูจน์ครั้งแรกในโลกว่า สามารถย้อนวัยได้จริงที่ระดับดีเอ็นเอ ไม่ใช่เพียงแค่ชะลอการแก่ชรา
ตัวชี้วัดความสำเร็จ #
การทำงานของตับ: กลับมาปกติ #
หนูแก่ที่ได้รับมณีแดงแสดง การทำงานของตับที่กลับมาปกติ โดยวัดจากระดับเอนไซม์ตับ (liver enzymes) และการสังเคราะห์โปรตีนของตับ ซึ่งบ่งชี้ว่าเซลล์ตับที่เสื่อมไปแล้วสามารถฟื้นฟูและทำงานได้เหมือนเดิม
ความจำ: ดีขึ้น #
การทดสอบความจำด้วย water maze test และ novel object recognition test พบว่าหนูที่ได้รับมณีแดงมี ความจำที่ดีขึ้นอย่างมีนัยสำคัญ เทียบเท่ากับหนูวัยหนุ่ม ซึ่งบ่งชี้ว่ามณีแดงสามารถเข้าสู่สมองและฟื้นฟูเซลล์ประสาทได้
จำนวนเซลล์แก่: ลดลง (จุดสีน้ำเงินลดลง) #
การย้อมสี SA-β-gal (Senescence-Associated β-galactosidase) ซึ่งเป็นตัวบ่งชี้เซลล์แก่ที่เชื่อถือได้ที่สุด พบว่า จำนวนเซลล์แก่ลดลงอย่างมาก ในทุกเนื้อเยื่อที่ตรวจสอบ รวมถึงตับ ไต และผิวหนัง จุดสีน้ำเงินที่บ่งชี้เซลล์แก่ลดลงอย่างเห็นได้ชัด
โปรตีนที่เกี่ยวข้องกับความชรา (H2AX, p16): ลดลง #
ระดับ γH2AX (histone ที่ถูกฟอสฟอรีเลตเมื่อเกิดความเสียหายของดีเอ็นเอ) และ p16 (ตัวบ่งชี้เซลล์แก่) ลดลงอย่างมีนัยสำคัญ ซึ่งบ่งชี้ว่าความเสียหายของดีเอ็นเอลดลงและเซลล์แก่ลดลงจริง
ไขมันในช่องท้อง: ลดลง #
หนูแก่ที่ได้รับมณีแดงมี ไขมันสะสมในช่องท้อง (visceral fat) ลดลง ซึ่งเป็นปัจจัยเสี่ยงสำคัญของโรค metabolic ต่างๆ การค้นพบนี้บ่งชี้ว่ามณีแดงสามารถฟื้นฟูการเผาผลาญพลังงานของร่างกายได้
พังผืดในตับ: หายไป #
พังผืดในตับ (liver fibrosis) ซึ่งเป็นภาวะที่เนื้อเยื่อปกติถูกแทนที่ด้วยเนื้อเยื่อแผลเป็น หายไปอย่างสมบูรณ์ หลังจากได้รับมณีแดง 2 เดือน นี่เป็นการพิสูจน์ว่ามณีแดงไม่เพียงแค่ย้อนวัย แต่สามารถ รักษาโรคที่เกิดจากความชราได้
รอยแยกดีเอ็นเอเยาว์: เพิ่มขึ้น #
ที่สำคัญที่สุด การตรวจวัดโดยตรงพบว่า ระดับ Youth-DNA-GAPs เพิ่มขึ้นอย่างมีนัยสำคัญ ในทุกเนื้อเยื่อที่ตรวจสอบ ซึ่งเป็นการยืนยันกลไกการทำงานที่ทีมวิจัยคาดการณ์ไว้
การทดลองในสัตว์ใหญ่ #
หมู: เนื้อมีคุณภาพดีขึ้น ปลอดภัยในสัตว์ใหญ่ #
การทดลองในหมูมีความสำคัญอย่างยิ่ง เพราะ สรีรวิทยาของหมูใกล้เคียงกับมนุษย์มากกว่าหนู ผลการทดลองพบว่าหมูที่ได้รับมณีแดงมี เนื้อมีคุณภาพดีขึ้น โดยเฉพาะความนุ่มและรสชาติ ซึ่งบ่งชี้ว่าการย้อนวัยที่ระดับเซลล์ส่งผลถึงระดับเนื้อเยื่อและอวัยวะ
ที่สำคัญคือ ไม่พบสารตกค้างที่เป็นอันตราย ในเนื้อหมูที่ได้รับมณีแดง ซึ่งเป็นการยืนยันความปลอดภัยของเทคโนโลยีนี้ในสัตว์ใหญ่ และเป็นข้อมูลสำคัญสำหรับการขออนุมัติทดลองในมนุษย์
ลิง: ผลลัพธ์เชิงบวก สนับสนุนการทดลองในมนุษย์ #
การทดลองในลิงกำลังดำเนินการ และผลเบื้องต้นแสดง ผลลัพธ์เชิงบวก ในการย้อนวัยและความปลอดภัย ลิงเป็นสัตว์ที่ใกล้ชิดกับมนุษย์มากที่สุดในการทดลองทางการแพทย์ ดังนั้นผลการทดลองในลิงจึงเป็น ขั้นตอนสุดท้ายก่อนการทดลองในมนุษย์
การรักษาโรคที่เกี่ยวข้อง #
พังผืดในตับ: หายขาด #
ตามที่กล่าวไว้ การทดลองในหนูพบว่า พังผืดในตับหายไปอย่างสมบูรณ์ หลังจากได้รับมณีแดง ซึ่งมีความหมายสำคัญเพราะพังผืดในตับเป็นภาวะที่ไม่สามารถรักษาให้หายขาดได้ด้วยวิธีการปัจจุบัน นอกจากการปลูกถ่ายตับ
แผลเบาหวาน: หายเร็วขึ้น #
การทดลองในหนูที่เป็นเบาหวานพบว่า แผลที่ผิวหนังหายเร็วขึ้นอย่างมีนัยสำคัญ หลังจากได้รับมณีแดง ซึ่งบ่งชี้ว่าการย้อนวัยของเซลล์ช่วยฟื้นฟูความสามารถในการซ่อมแซมของร่างกาย
ศักยภาพในการรักษา: โรคอัลไซเมอร์, พังผืดปอดหลังโควิด, หลอดเลือดแข็ง #
จากกลไกการทำงานและผลการทดลองที่ได้ ทีมวิจัยเห็นศักยภาพของมณีแดงในการรักษาโรคต่างๆ ที่เกี่ยวข้องกับความชรา:
| โรค | กลไกที่มณีแดงอาจช่วย | สถานะการวิจัย |
|---|---|---|
| โรคอัลไซเมอร์ | ฟื้นฟูเซลล์ประสาท ลดการสะสมของเบต้า-อะมิลอยด์ | การทดลองในสัตว์แสดงผลเชิงบวก |
| พังผืดปอดหลังโควิด | ย้อนวัยเซลล์ปอด ลดการอักเสบเรื้อรัง | อยู่ระหว่างการศึกษา |
| หลอดเลือดแข็ง | ฟื้นฟูเซลล์หลอดเลือด ลดการสะสมของคราบพลัค | อยู่ระหว่างการศึกษา |
| มะเร็งที่เกี่ยวข้องกับอายุ | ลดความเสียหายของดีเอ็นเอที่นำไปสู่มะเร็ง | ศึกษาเบื้องต้น |
สถานะปัจจุบันและอนาคต #
ขั้นตอนการพัฒนา #
ระยะที่ 1: ค้นพบกลไกและทดสอบในหลอดทดลอง #
ระยะที่ 1 ของโครงการดำเนินการเสร็จสิ้นแล้ว โดยมีการ ค้นพบกลไกพื้นฐานของการแก่ของดีเอ็นเอ และ พิสูจน์ว่า Box A สามารถสร้างรอยแยกดีเอ็นเอเยาว์ได้ ในหลอดทดลอง ผลงานได้รับการตีพิมพ์ในวารสารระดับนานาชาติ FASEB BioAdvances และ Systematic Reviews in Pharmacy
ระยะที่ 2: ทดสอบในสัตว์ทดลอง (หนู, หมู, ลิง) #
ระยะที่ 2 กำลังดำเนินการอยู่ โดยมีการทดสอบในหนูเสร็จสิ้นแล้วด้วยผลที่น่าพอใจ การทดสอบในหมูเสร็จสิ้นแล้วเช่นกัน ยืนยันความปลอดภัยในสัตว์ใหญ่ การทดสอบในลิงกำลังดำเนินการ และคาดว่าจะเสร็จสิ้นในเร็วๆ นี้
ระยะที่ 3: ทดลองทางคลินิกในมนุษย์ (กำลังดำเนินการ) #
ระยะที่ 3 คือ การทดลองทางคลินิกในมนุษย์ (clinical trials) ซึ่งจะแบ่งเป็น 3 เฟส:
- เฟส 1: ทดสอบความปลอดภัยในผู้สมัครอาสาสมัครจำนวนน้อย (20-80 คน)
- เฟส 2: ทดสอบประสิทธิภาพในผู้ป่วยที่มีโรคเฉพาะ (100-300 คน)
- เฟส 3: ทดสอบประสิทธิภาพและความปลอดภัยในวงกว้าง (1,000-3,000 คน)
คาดว่าการทดลองเฟส 1 จะเริ่มได้ใน ปี 2025-2026 หากได้รับการอนุมัติจากหน่วยงานกำกับดูแล
ความร่วมมือกับภาคอุตสาหกรรม #
บันทึกข้อตกลงกับ ปตท. จำกัด (มหาชน) #
ความร่วมมือกับ บริษัท ปตท. จำกัด (มหาชน) ลงนามเมื่อวันที่ 23 กันยายน 2565 มีวัตถุประสงค์เพื่อ:
- พัฒนาเทคโนโลยีมณีแดงสู่ระดับอุตสาหกรรม
- สร้างมาตรฐานการผลิตที่ได้รับการรับรองระหว่างประเทศ (GMP)
- วางแผนการตลาดและการจัดจำหน่ายทั้งในประเทศและต่างประเทศ
เป้าหมาย: พัฒนาเป็นผลิตภัณฑ์รักษาโรคและย้อนวัย #
เป้าหมายระยะยาวคือการพัฒนามณีแดงให้เป็นผลิตภัณฑ์ที่สามารถใช้ได้จริงในโรงพยาบาล โดยมีแผนพัฒนา 2 สาย:
- สายที่ 1: ยาฉีดสำหรับรักษาโรคที่เกี่ยวข้องกับความชรา (เช่น พังผืดในตับ, โรคอัลไซเมอร์)
- สายที่ 2: ผลิตภัณฑ์เสริมอาหารหรือยาสำหรับการย้อนวัยเชิงป้องกัน
สร้างรายได้ให้ประเทศไทย #
ศ.อภิวัฒน์ตั้งเป้าหมายว่ามณีแดงจะกลายเป็น “เครื่องกำเนิดรายได้ให้กับประเทศไทย” โดยไม่ต้องพึ่งพาเทคโนโลยีจากต่างประเทศ ตลาดต้านความชราทั่วโลกมีมูลค่ากว่า 200,000 ล้านดอลลาร์สหรัฐ และคาดว่าจะเติบโตอย่างต่อเนื่อง หากมณีแดงสามารถครองส่วนแบ่งการตลาดแม้เพียงเล็กน้อย ก็จะสร้างรายได้มหาศาลให้กับประเทศ
ความคาดหวังในอนาคต #
การทดลองทางคลินิกระยะที่ 1-3 #
การทดลองทางคลินิกจะใช้เวลาประมาณ 5-10 ปี ตั้งแต่เฟส 1 จนถึงการขึ้นทะเบียนเป็นยา โดยมีกำหนดการโดยประมาณดังนี้:
| เฟส | กิจกรรม | ระยะเวลา | เป้าหมาย |
|---|---|---|---|
| เฟส 1 | ทดสอบความปลอดภัย | 1-2 ปี | หาขนาดยาที่ปลอดภัย |
| เฟส 2 | ทดสอบประสิทธิภาพ | 2-3 ปี | ยืนยันประสิทธิภาพในโรคเฉพาะ |
| เฟส 3 | ทดสอบในวงกว้าง | 3-5 ปี | เปรียบเทียบกับมาตรฐานการรักษา |
การขึ้นทะเบียนเป็นยา #
หลังจากเสร็จสิ้นการทดลองทางคลินิก จะต้องยื่นขอขึ้นทะเบียนเป็นยาต่อ สำนักงานคณะกรรมการอาหารและยา (อย.) ของไทย และ องค์การอาหารและยานานาชาติ (FDA) ของสหรัฐอเมริกาและยุโรป กระบวนการนี้อาจใช้เวลาเพิ่มอีก 1-2 ปี
การใช้งานจริงในโรงพยาบาล #
คาดว่ามณีแดงจะสามารถใช้งานจริงในโรงพยาบาลได้ใน ปี 2030-2035 หากทุกอย่างเป็นไปตามแผน โดยจะเริ่มจากการใช้ในโรงพยาบาลขนาดใหญ่ที่มีศักยภาพในการติดตามผล และขยายไปสู่โรงพยาบาลทั่วไปในระยะต่อไป
คำถามที่พบบ่อย (FAQ) #
คำถามเชิงเทคนิค #
มณีแดงต่างจากยาต้านความชราอื่นอย่างไร? #
| ลักษณะ | ยาต้านความชราอื่นๆ | มณีแดง (RED-GEMs) |
|---|---|---|
| กลไกการทำงาน | ซ่อมแซมความเสียหายที่เกิดแล้ว / กำจัดเซลล์แก่ | สร้างรอยแยกดีเอ็นเอเยาว์ ป้องกันไม่ให้เกิดความเสียหาย |
| เป้าหมาย | ชะลอการแก่ชรา | ย้อนวัยให้กลับมาอ่อนเยาว์ |
| ระดับการทำงาน | ระดับเซลล์หรืออวัยวะ | ระดับดีเอ็นเอ (พื้นฐานที่สุด) |
| ความปลอดภัย | บางชนิดมีผลข้างเคียง | ใช้โปรตีนธรรมชาติ ปลอดภัยสูง |
| ฐานวิจัย | พัฒนาต่อเนื่องจากทฤษฎีเดิม | ทฤษฎีใหม่ที่ค้นพบโดยคนไทย |
ทำไมต้องเป็น Box A ทำไมไม่ใช้ Box B หรือ HMGB1 ทั้งโมเลกุล? #
Box A ถูกเลือกใช้เพราะ:
- มี กิจกรรมสร้างรอยแยกดีเอ็นเอเยาว์ สูง
- ไม่มีฤทธิ์กระตุ้นการอักเสบ แต่กลับมีฤทธิ์ ยับยั้งการอักเสบ (antagonist)
- มี Nuclear Localization Signal (NLS) ที่ตำแหน่ง 28-44 นำเข้าสู่นิวเคลียสได้อย่างมีประสิทธิภาพ
Box B ไม่ถูกเลือกใช้เพราะ:
- ไม่มีกิจกรรมสร้างรอยแยกดีเอ็นเอเยาว์
- มี ฤทธิ์กระตุุ้นการอักเสบรุนแรง ผ่านการจับกับ TLR4 และ RAGE
- อาจก่อให้เกิด ภาวะอักเสบเรื้อรัง ที่เป็นอันตราย
HMGB1 ทั้งโมเลกุลไม่ถูกเลือกใช้เพราะ:
- มี Box B ผสมอยู่ จึงมี ฤทธิ์กระตุ้นการอักเสบ
- มีหางกรดที่ ลดความสามารถในการจับดีเอ็นเอ
- ขนาดโมเลกุลใหญ่ ทำให้ ส่งเข้าเซลล์ได้ยากกว่า
รอยแยกดีเอ็นเอ (DNA gaps) ไม่ใช่ความเสียหายหรือ? #
ไม่ใช่ — นี่คือจุดสำคัญที่ทีมวิจัยไทยค้นพบ:
| ลักษณะ | รอยแยกจากความเสียหาย | Youth-DNA-GAPs (รอยแยกเยาว์) |
|---|---|---|
| สาเหตุ | รังสี สารเคมี ความผิดพลาดในการจำลอง | กระบวนการธรรมชาติที่ควบคุมได้ |
| ผลที่มีต่อเซลล์ | กระตุ้น DDR อาจทำให้เซลล์ตาย | ถูกซ่อนโดย histone deacetylation ไม่กระตุ้น DDR |
| หน้าที่ | ไม่มีหน้าที่ เป็นความเสียหาย | ลดแรงบิดเกลียว ป้องกันความเสียหาย |
| ระดับในเซลล์อ่อนเยาว์ | ต่ำ | สูง |
| ระดับในเซลล์แก่ | สูง (สะสม) | ต่ำ (สูญเสีย) |
รอยแยกดีเอ็นเอเยาว์เปรียบเสมือน “ข้อต่อ” หรือ “ช่องว่างในรางรถไฟ” ที่ช่วยให้โครงสร้างมีความยืดหยุ่นและไม่เสียหายเมื่อมีแรงกระทำ
มณีแดงทำงานกับเซลล์ทุกชนิดหรือไม่? #
จากการศึกษาจนถึงปัจจุบัน มณีแดงสามารถทำงานกับเซลล์หลายชนิด ที่ทดสอบ รวมถึง:
- เซลล์ตับ (hepatocytes)
- เซลล์ไต (kidney cells)
- เซลล์ประสาท (neurons)
- เซลล์ผิวหนัง (fibroblasts)
- เซลล์กล้ามเนื้อ (myocytes)
อย่างไรก็ตาม ประสิทธิภาพอาจแตกต่างกันไปตามประเภทของเซลล์และสภาวะของเซลล์ การศึกษาเพิ่มเติมกำลังดำเนินการเพื่อระบุประเภทเซลล์ที่ตอบสนองดีที่สุด
คำถามเชิงปฏิบัติ #
ตอนนี้สามารถใช้มณีแดงได้แล้วหรือยัง? #
ยังไม่สามารถใช้ได้ — มณีแดงอยู่ในระหว่างการพัฒนาและยังไม่ได้รับการอนุมัติจากหน่วยงานกำกับดูแลใดๆ
| ระยะ | กิจกรรม | สถานะ |
|---|---|---|
| ระยะที่ 1 | ค้นพบกลไกและทดสอบในหลอดทดลอง | ✅ เสร็จสิ้น |
| ระยะที่ 2 | ทดสอบในสัตว์ทดลอง (หนู, หมู, ลิง) | 🔄 ใกล้เสร็จสิ้น |
| ระยะที่ 3 | ทดลองทางคลินิกในมนุษย์ | ⏳ ยังไม่เริ่ม (คาด 2025-2026) |
| การขึ้นทะเบียน | ขออนุมัติจาก อย. และ FDA | ⏳ รอผลการทดลอง |
| การใช้งานจริง | ใช้ในโรงพยาบาล | ⏳ คาด 2030-2035 |
คำเตือน: หากมีผู้แอบอ้างขายมณีแดงในขณะนี้ เป็นการหลอกลวงแน่นอน เนื่องจากผลิตภัณฑ์ยังไม่มีวางจำหน่าย
ใครบ้างที่อาจได้ประโยชน์จากมณีแดงในอนาคต? #
กลุ่มผู้ที่อาจได้ประโยชน์จากมณีแดงในอนาคต แบ่งตามระดับความเร่งด่วน:
ระดับเร่งด่วน (การรักษาโรค):
- ผู้ป่วย พังผืดในตับ ที่ไม่ตอบสนองต่อการรักษาปัจจุบัน
- ผู้ป่วย โรคอัลไซเมอร์ ในระยะเริ่มต้น
- ผู้ป่วย พังผืดปอดหลังโควิด
- ผู้ป่วย แผลเบาหวาน ที่หายช้า
ระดับป้องกัน (การย้อนวัย):
- ผู้สูงอายุที่ต้องการ รักษาสุขภาพและคุณภาพชีวิต
- ผู้ที่มี ปัจจัยเสี่ยงโรคเรื้อรัง ที่เกี่ยวข้องกับความชรา
- ผู้ที่ต้องการ ฟื้นฟูร่างกายหลังจากการรักษาโรค
มณีแดงมีผลข้างเคียงหรือไม่? #
จากการทดสอบในสัตว์จนถึงปัจจุบัน ไม่พบผลข้างเคียงที่เป็นอันตราย อย่างไรก็ตาม ผลข้างเคียงที่อาจเกิดขึ้นในอนาคตเมื่อใช้ในมนุษย์ อาจรวมถึง:
| ผลข้างเคียงที่เป็นไปได้ | ความรุนแรง | ความน่าจะเป็น |
|---|---|---|
| การตอบสนองภูมิคุ้มกันต่อ plasmid | เบา | ต่ำ |
| การสะสมของแคลเซียมฟอสเฟต | เบา | ต่ำ |
| การสร้างรอยแยกมากเกินไป | ไม่ทราบ | ต่ำ (มีกลไกควบคุม) |
การทดลองทางคลินิกจะช่วยระบุผลข้างเคียงที่อาจเกิดขึ้นในมนุษย์อย่างละเอียด
ราคาของการรักษาด้วยมณีแดงจะสูงแค่ไหน? #
ราคายังไม่สามารถระบุได้ในขณะนี้ เนื่องจากยังอยู่ในระหว่างการพัฒนา แต่ทีมวิจัยมีเป้าหมายที่จะทำให้ มณีแดงเข้าถึงได้สำหรับประชาชนทั่วไป โดย:
- ใช้ เทคโนโลยีการผลิตที่มีต้นทุนต่ำ (Calcium Phosphate nanoparticle แทน lipid nanoparticle ที่แพงกว่า)
- พัฒนา กระบวนการผลิตในประเทศ ลดการพึ่งพานำเข้า
- สร้าง economy of scale จากการผลิตในปริมาณมาก
คาดการณ์เบื้องต้นว่าราคาอาจอยู่ในระดับ หลักพันถึงหลักหมื่นบาทต่อการรักษา ขึ้นอยู่กับขนาดยาและความถี่ในการให้ ซึ่งถูกกว่ายาต้านความชราบางชนิดที่พัฒนาในต่างประเทศ
คำถามเกี่ยวกับการวิจัย #
ผลการทดลองในหนูสามารถใช้กับมนุษย์ได้เลยหรือไม่? #
ไม่สามารถใช้ได้โดยตรง — ผลการทดลองในหนูเป็นเพียงขั้นตอนแรกในการพิสูจน์หลักการและความปลอดภัยเบื้องต้น ก่อนที่จะนำไปใช้ในมนุษย์ ต้องผ่านการทดสอบในสัตว์ที่ใกล้ชิดกับมนุษย์มากขึ้น (หมู, ลิง) และการทดลองทางคลินิกในมนุษย์อย่างเข้มงวน
อย่างไรก็ตาม ความสำเร็จในหนูเป็น สัญญาณที่ดี เพราะ:
- กลไกการแก่ของดีเอ็นเอ ถูกอนุรักษ์ไว้ตลอดวิวัฒนาการ ตั้งแต่ยีสต์ไปจนถึงมนุษย์
- Box A ของ HMGB1 มี ลำดับกรดอะมิโนที่คล้ายกันมาก ระหว่างสปีชีส์ต่างๆ
- การทดสอบในหมูและลิงกำลัง ยืนยันความปลอดภัยและประสิทธิภาพ ในสัตว์ที่ใกล้เคียงมนุษย์มากขึ้น
มีการตีพิมพ์วิจัยในวารสารระดับนานาชาติหรือไม่? #
ใช่ — ผลงานวิจัยของทีมศ.อภิวัฒน์ได้รับการตีพิมพ์ในวารสารระดับนานาชาติที่ผ่านการตรวจสอบโดยผู้เชี่ยวชาญ (peer-reviewed) หลายฉบับ:
| วารสาร | ปี | หัวข้อ | ความสำคัญ |
|---|---|---|---|
| FASEB BioAdvances | 2022 | The roles of HMGB1-produced DNA gaps in DNA protection and aging biomarker reversal | รายงานแรกของกระบวนการป้องกันดีเอ็นเอตามธรรมชาติที่ป้องกันการแก่ |
| Systematic Reviews in Pharmacy | 2023 | Box A of HMGB1 Producing DNA Gaps: A Remedy for the DNA Protection and Rejuvenation Effects | บทความรีวิวกลไกและศักยภาพทางการรักษา |
| ScienceAsia | 2023 | บทความที่เกี่ยวข้อง | การพัฒนาเทคโนโลยี |
| BMC Pulmonary Medicine | 2025 | HMGB1 Box A gene therapy to alleviate bleomycin-induced pulmonary fibrosis in rats | การรักษาพังผืดปอด |
| PLOS ONE | 2025 | HMGB1-BoxA gene therapy in reversing cisplatin resistance in human lung cancer cells | การกลับเซลล์มะเร็งให้ตอบสนองต่อยา |
ทีมวิจัยไทยได้รับการยอมรับจากต่างประเทศอย่างไร? #
การค้นพบของทีมวิจัยไทยได้รับการยอมรับจากชุมชนวิทยาศาสตร์ระหว่างประเทศว่าเป็น “รายงานแรกของกระบวนการป้องกันดีเอ็นเอตามธรรมชาติที่ป้องกันการแก่” (the first report of a naturally occurring DNA protection process preventing aging)
ความได้เปรียบสำคัญของทีมวิจัยไทยคือ:
- ทฤษฎีใหม่นี้ไม่มีอยู่ในต่างประเทศ — ยาต้านความชราที่พัฒนาในต่างประเทศล้วนออกฤทธิ์ต่อเนื่องจากกลไกของทฤษฎีใหม่นี้ แต่ไม่ได้แก้ไขที่ต้นเหตุ
- มณีแดงออกฤทธิ์ที่ต้นเหตุ — จึงมีศักยภาพในการย้อนวัยได้สมบูรณ์กว่าวิธีอื่น
- สิทธิบัตรและทรัพย์สินทางปัญญา — เป็นของทีมวิจัยไทย ไม่ต้องเสียค่าลิขสิทธิ์ให้ต่างชาติ
สรุป #
ความสำคัญของการค้นพบ #
ทฤษฎีใหม่ที่อธิบายการแก่ของดีเอ็นเอเป็นครั้งแรกในโลก #
การค้นพบของศ.ดร.นพ. อภิวัฒน์ มุทิรางกูร และทีมวิจัยเป็นครั้งแรกในโลกที่มีการ อธิบายกลไกพื้นฐานของการแก่ของดีเอ็นเอ อย่างสมบูรณ์ ทฤษฎีนี้เปลี่ยนแปลงความเข้าใจที่มีมายาวนานว่าความชราเป็นเพียงผลจากการสะสมของความเสียหายตามเวลา เป็นการมองว่า ความชราเป็นกระบวนการที่ควบคุมได้ ซึ่งเกิดจากการขาดแคลนโครงสร้างที่จำเป็นต่อการปกป้องดีเอ็นเอ
ความรู้นี้ไม่มีอยู่ในต่างประเทศ ทำให้ประเทศไทยมี ความได้เปรียบเชิงกลยุทธ์ ในการพัฒนานวัตกรรมด้านนี้ก่อนใคร ไม่ต้องพึ่งพาเทคโนโลยีหรือทฤษฎีจากต่างชาติ
นวัตกรรมจากฝีมือคนไทย ไม่ต้องพึ่งพาต่างชาติ #
มณีแดงเป็น นวัตกรรมที่คิดค้น วิจัย และพัฒนาโดยคนไทย ตั้งแต่ต้นจนจบ ตั้งแต่การค้นพบทฤษฎีพื้นฐาน การออกแบบโมเลกุล การทดสอบในห้องปฏิบัติการ ไปจนถึงการพัฒนาสู่ระดับอุตสาหกรรม ความสำเร็จนี้แสดงให้เห็นว่า ประเทศไทยมีศักยภาพในการเป็นผู้นำด้านวิทยาศาสตร์และเทคโนโลยีระดับโลก
ศักยภาพในการเปลี่ยนแปลงวงการแพทย์ #
จากการรักษาโรคสู่การป้องกันและย้อนวัย #
มณีแดงมีศักยภาพในการ เปลี่ยนแปลงวิธีการดูแลสุขภาพ จากเดิมที่มุ่งเน้นการรักษาโรคหลังจากเกิดขึ้น เป็นการ ป้องกันไม่ให้โรคเกิด และย้อนวัยร่างกายให้กลับมาแข็งแรง นี่เป็นการเปลี่ยนแปลงครั้งสำคัญในวงการแพทย์ที่อาจส่งผลกระทบต่อวิธีการดำเนินชีวิตของมนุษยชาติในอนาคต
ลดภาระโรคเรื้อรังที่เกี่ยวข้องกับความชรา #
โรคที่เกี่ยวข้องกับความชรา เช่น เบาหวาน โรคหัวใจ โรคสมองเสื่อม และมะเร็ง เป็นภาระหลักของระบบสาธารณสุขทั่วโลก หากมณีแดงสามารถ ชะลอหรือย้อนกลับกระบวนการชรา ได้จริง จะสามารถ ลดภาระการรักษาพยาบาลอย่างมหาศาล และเพิ่มคุณภาพชีวิตของผู้สูงอายุได้อย่างมีนัยสำคัญ
ข้อควรระวังและความหวัง #
ต้องรอผลการทดลองทางคลินิกอย่างละเอียด #
แม้ผลการทดสอบในสัตว์จะน่าพอใจ แต่ ความปลอดภัยและประสิทธิภาพในมนุษย์ต้องได้รับการพิสูจน์อย่างเข้มงวน ผ่านการทดลองทางคลินิกหลายเฟส ซึ่งอาจใช้เวลา 5-10 ปี ประชาชนควรระวังไม่หลงเชื่อผู้ที่แอบอ้างขายมณีแดงในขณะนี้
ความหวัง: คนไทยจะมีสุขภาพดีที่เลือกได้ ไม่แก่ตามวัย #
ความหวังสูงสุดของทีมวิจัยคือ คนไทยและมนุษยชาติจะมีสุขภาพดีที่เลือกได้ — ไม่ต้องยอมรับความชราและโรคที่เกิดจากความชราเป็นสิ่งที่หลีกเลี่ยงไม่ได้ แต่สามารถ ควบคุมและย้อนกลับได้ มณีแดงไม่ใช่ “ยาอายุวัฒนะ” ที่ทำให้เป็นอมตะ แต่เป็น นวัตกรรมที่ช่วยให้ร่างกายแข็งแรงและมีคุณภาพชีวิตที่ดีได้นานขึ้น ตามที่แต่ละคนเลือก
บทความนี้รวบรวมข้อมูลจากผลงานวิจัยของศ.ดร.นพ. อภิวัฒน์ มุทิรางกูร และทีมวิจัยจากคณะแพทยศาสตร์ จุฬาลงกรณ์มหาวิทยาลัย ที่ตีพิมพ์ในวารสารระดับนานาชาติ และข้อมูลจากการให้สัมภาษณ์ของศ.อภิวัฒน์ต่อสื่อมวลชน





